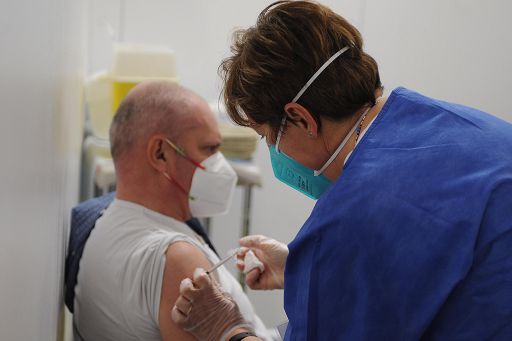
Procedura accelerata in vista di campagne vaccinali autunno-inverno
Roma, 1 set. (askanews) – La Commissione europea ha autorizzato il vaccino anti COVID-19 Comirnaty, adattato nei confronti della variante XBB.1.5, sviluppato da BioNTech-Pfizer. Questo vaccino – nota la Commissione – segna un nuovo importante traguardo nella lotta contro la malattia: si tratta del terzo adattamento del vaccino per far fronte alle nuove varianti della Covid-19.
Il vaccino è autorizzato per gli adulti, i bambini e i neonati di oltre 6 mesi. In linea con le precedenti raccomandazioni dell’EMA e del Centro europeo per la prevenzione e il controllo delle malattie (ECDC), agli adulti e ai bambini di almeno 5 anni da vaccinare dovrebbe essere somministrata un’unica dose, indipendentemente dalla loro anamnesi vaccinale in relazione alla Covid-19.
L’autorizzazione è stata rilasciata dopo una rigorosa valutazione da parte dell’Agenzia europea per i medicinali nell’ambito del meccanismo di valutazione accelerata. La Commissione ha autorizzato questo vaccino adattato seguendo una procedura accelerata per consentire agli Stati membri di prepararsi in tempo utile alle rispettive campagne di vaccinazione autunno-invernali.